光酸染料(Photoacid Generator Dyes, PAG)作为光控pH调节及质子释放的关键分子工具,已广泛应用于电子化学品(如光刻胶)等高端制造领域。近年来,以光酸染料为工具的多学科研究(如智能材料、生物医药)逐步兴起,突破了光酸染料的传统应用边界。然而,现有的光酸染料(PAG)在多学科交叉应用过程中存在一定的局限性:一方面,商品化的PAG分子激发波长集中在紫外或深蓝光区域,严重阻碍了其在多领域的应用研究范围(特别是生物医药领域);另一方面,传统光酸染料功能单一,往往只注重酸的释放,而其互补分子单元往往被认为是反应过程的“废弃物”,原子利用率低下。
针对上述问题,我校化学与分子工程学院张隽佶教授团队发展了系列红光响应的新型有机光酸染料分子体系(PBI-PAG),相关工作以“All-in-One Photoacid Generators with Green/Red-light Responsiveness and Cooperative Functionality”为题发表于国际著名学术期刊《德国应用化学》(Angew. Chem. Int. Ed., 2025, e202425313)。
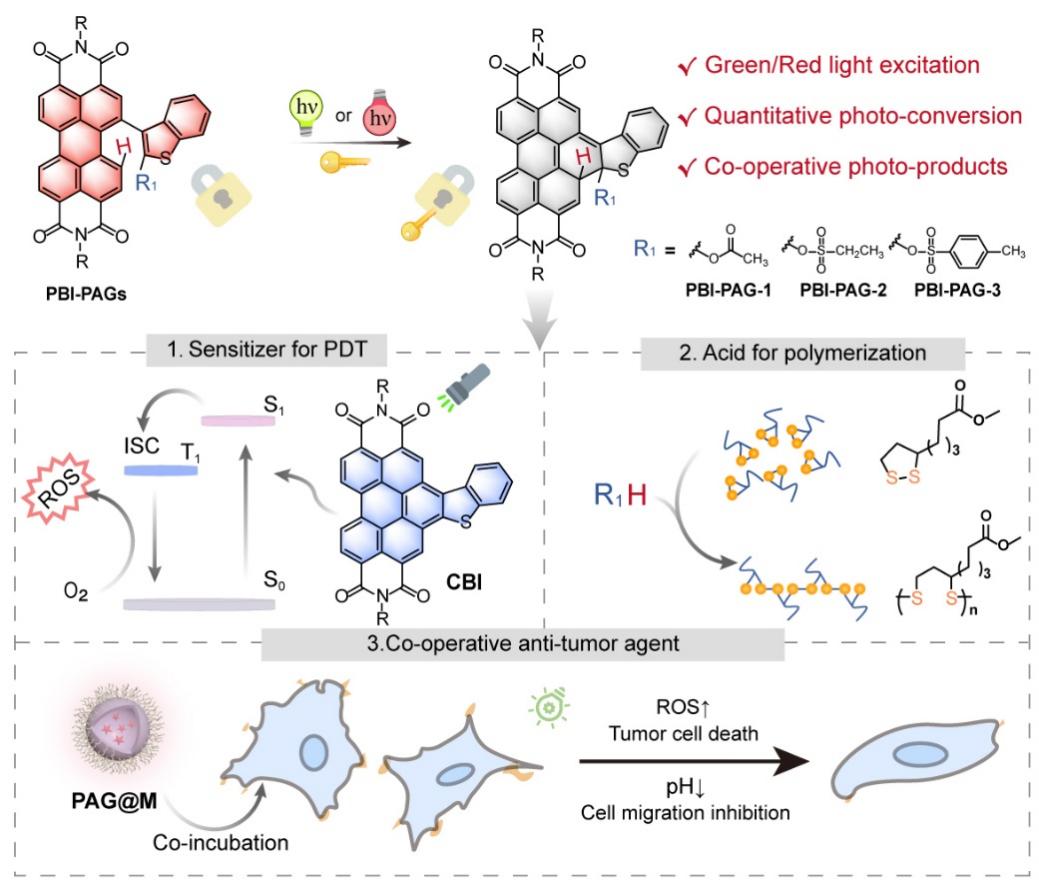
与传统PAG分子相比,该新型光酸染料可实现全光谱(254 nm – 605 nm,紫外-红光)光响应放酸,具有较高的光释放效率(фε(λmax) ~ 300 M-1 cm-1),以及近乎当量反应的高光转化率(> 99.3%)。更重要的是,除了光诱导质子酸生成外,光反应生成的另一部分蒄类衍生物(CBI)具有光敏剂的功能,首次报道了具有协同多功能单元的光酸染料分子体系。研究表明,PBI-PAG首先经由己三烯6π光环化形成环化中间体,通过随后的消除反应释放酸与光敏剂,高度特异的光反应过程有效抑制了光副产物的生成,大幅提升了反应的专一性及原子利用率。
PBI-PAG同时展现了多科学领域交叉应用研究的潜力。首先,仅通过添加0.08% w/w的PBI-PAG即可通过原位红光释酸,引发硫辛酸酯(TA-Me)聚合,体现了PBI-PAG在光聚合功能材料领域的潜在应用价值;其次,我们验证了所释放的CBI光敏剂作为光动力治疗试剂对铜绿假单胞菌(p.aeruginosa)的杀菌抗菌效果。在此基础上,基于多功能红光光酸染料1:1当量光释放质子酸和光敏剂的特点,制备了光酸胶束试剂并与肿瘤细胞共孵育。质子酸的释放能够诱导肿瘤细胞中黏着斑基酶(Focal adhesion kinase, FAK)中组氨酸(FAK-His58)的质子化,从而中断酪氨酸(FAK-Tyr397)磷酸化及后续基酶激活通路,抑制细胞的迁移行为。实验结果表明,孵育了光酸胶束的肿瘤细胞在红光照射下黏着斑蛋白的表达和伪足的生成显著下降,细胞迁移能力仅为光照前的1/10;而同时释放的光敏剂则在红光照射下对肿瘤细胞活性的抑制率超过70%,起到了光动力学治疗的效果。多元协同功能的红光光酸染料广阔的生物应用前景为肿瘤的光协同治疗提供了新的方法和思路。
该论文共同第一作者为华东理工大学博士生郭慧超、特聘副研究员张志伟,通讯作者为张隽佶教授。该工作在田禾院士的悉心指导下完成,并得到了国家优秀青年科学基金、国基金面上项目、上海市科委原创探索项目等资金的支持。