癌症严重威胁着人类的健康和生命,其发病率和死亡率逐年上升。发展肿瘤治疗的新原理、新方法,提高治疗效果,并降低副作用,是当前生命化学和医学领域亟待解决的关键科学问题。近日,华东理工大学钱若灿副教授与伊利诺伊州大学香槟分校陆艺教授合作,设计了一种基于DNAzyme分子机器的肿瘤复合治疗策略,可同时调控T细胞/癌细胞间相互作用以及诱导肿瘤细胞内线粒体聚集,促使肿瘤细胞凋亡。相关成果以“Combination Cancer Treatment: Using Engineered DNAzyme Molecular Machines for Dynamic Inter- and Intracellular Regulation”为题发表于德国应用化学(Angew. Chem. Int. Ed. 2022, DOI: https://doi.org/10.1002/anie.202210935)。
近年来,肿瘤复合治疗作为一种高效癌症杀伤策略,取得了飞速发展,具有良好的应用前景。尽管如此,开发对正常细胞无毒的靶向复合治疗方法仍是一项挑战。金属离子特异激活的DNAzyme在细胞调控方面具有独特优势,被广泛用于细胞相关研究。在之前的工作中,双方团队基于金属离子特异性的DNAzyme和相关底物构建细胞调控模块,设计了多种逻辑控制开关,实现了细胞间动态行为的人工调控,包括单个细胞和多细胞球体的细胞间连接与解离(J. Am. Chem. Soc., 2021, 143, 5737-5744)。但上述工作采用胆固醇作为锚定剂,缺乏肿瘤靶向能力。
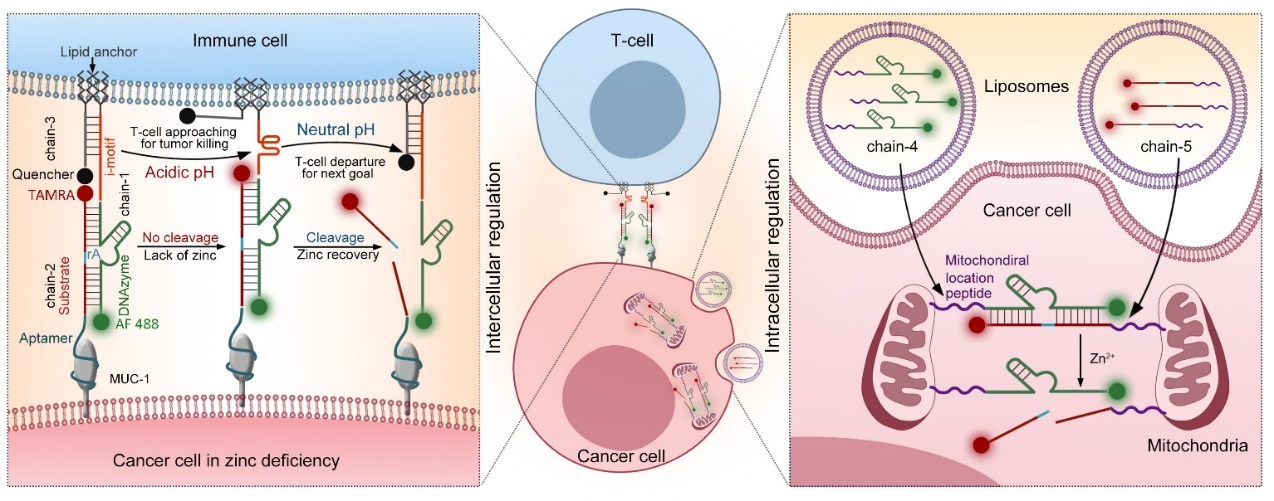
为了克服以上限制,本工作将MUC-1适配体、i-motif结构域、线粒体靶向模块与DNAzyme结构藕连,构建了具备细胞间与细胞内调控功能的DNAzyme分子机器,可分别从细胞外与细胞内对肿瘤细胞进行靶向杀伤。在细胞外,本策略可实现T细胞与肿瘤细胞间的动态调控,包括肿瘤细胞识别、T细胞-肿瘤细胞密接以及肿瘤杀伤后的T细胞解离。在乏锌肿瘤细胞内,DNAzyme分子机器可诱导线粒体聚集,产生ROS并促进肿瘤细胞凋亡。在酸性环境下,凋亡荧光成像实验证明基于DNAzyme分子机器的肿瘤复合治疗策略对乏锌PANC-1细胞的杀伤效果显著。
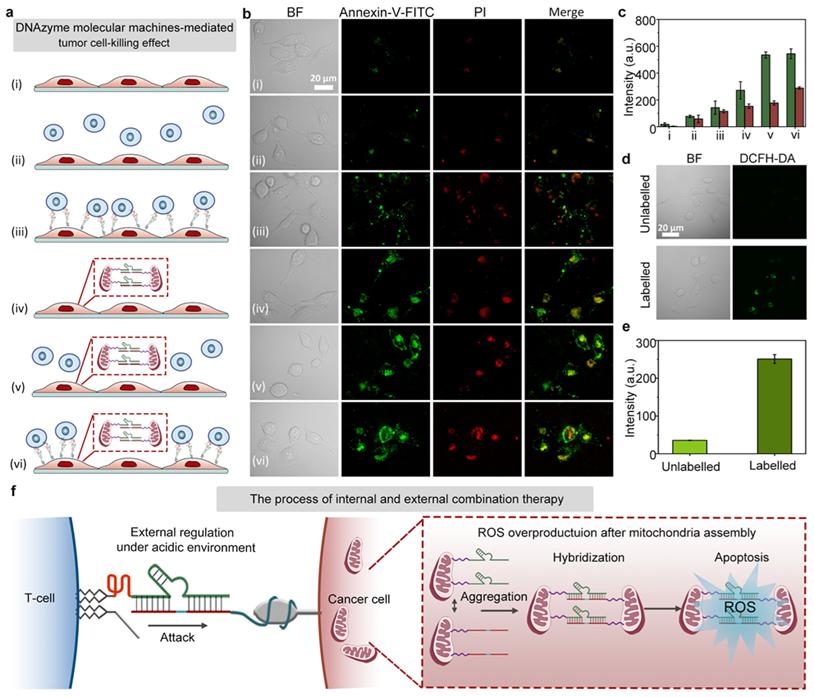
本研究展示了一种基于DNAzyme分子机器的细胞动态调控方法,为肿瘤联合治疗提供了新策略。上述研究工作由华东理工大学博士研究生周泽蕊在钱若灿副教授和陆艺教授指导下完成。共同第一作者为钱若灿副教授和周泽蕊,共同通讯作者为钱若灿副教授和陆艺教授。该工作得到了李大伟教授的建议和帮助,并得到了结构可控先进功能材料及其制备教育部重点实验室、费林加诺贝尔奖科学家联合研究中心的支持以及国家自然科学基金、国家科技重大专项等项目资助。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202210935