| 王爱勇副教授Applied Catalysis B: Environmental:原位DRIFTS研究NO的捕获机制 |
 1 摘要简介 Co-Ni双金属水合氧化物应用于半封闭空间低浓度一氧化氮(NO)污染的治理。通过表面积/孔隙率分析仪、SEM/TEM成像和元素图谱对这些材料的织构进行了表征。应用原位DRIFTS、XPS和程序升温脱附等方法研究了NO的捕获机制。通过在环境温度下使O2/He中的低浓度NO流过这些材料来测试NO存储容量。Co/Ni摩尔比极大地影响了Co-Ni双金属水合氧化物的表面积、孔结构和形态,从而影响了低浓度NO的去除性能。在NO储存过程中,发现亚硝酸盐的形成与Co有关,硝酸盐的形成与Ni有关,当Co上形成的亚硝酸盐被Ni上的晶格氧进一步氧化为硝酸盐时,存在协同作用。最后,这些材料很容易通过用Na2S2O8水溶液洗涤而再生。 2 背景介绍 尽管运输业正在迅速从传统燃料向电气化发展,但目前大多数重型道路运输仍依赖化石燃料驱动的内燃机。因此,即使部署了高效的NOx减排技术,例如贫NOx捕集器(LNT)和选择性催化还原(SCR),发动机排气中存在的NOx(氮氧化物,主要是NO)在不久的将来仍将是空气污染的主要来源。特别是,这种技术在所谓的“冷启动”条件下效率低下。随着世界经济的不断繁荣,对室内停车场和公路隧道的需求不断增加,尤其是在大都市地区。在这样的半封闭空间中,来自发动机排气的NOx很容易积聚在空气中。如果不加以处理,NOx浓度可能达到数十ppm,这被认为是严重的环境和人类健康危害。由于两个主要的技术挑战,包括(1)要处理的大量空气,以及(2)这种类型的空气污染所固有的低NOx浓度,用于消除空气中低浓度NOx的高效和经济的技术尚未实现。 3 图文解析 图1a显示了在环境温度下,与具有不同Co/Ni摩尔比(表示为CoxNiyOz·nH2O)的纯Co、纯Ni和Co-Ni含水氧化物相比,低浓度NO去除率作为运行时间的函数。实时NO和NO2出口浓度也包括在图1b中。纯Co显示出显著的NO捕获效率,其中100%的NO消除持续约18 h。当NO去除率降至100%以下时(即,当NO出现在出口中时),在出口中未检测到NO2。与之形成鲜明对比的是,纯Ni显示出较差的NO捕获,其中100%的NO消除仅持续几分钟。此外,随着NO捕获效率的下降,~2 ppm NO2在出口中检测到,对应于8.9*10−7mol·g−1·min−1的NO2形成率。这表明,与纯Co相比,纯Ni在催化NO氧化为NO2方面具有活性。对于CoxNiyOz·nH2O材料,观察到Co/Ni比的显著影响。Co4Ni1显示在~28h内100% NO消除。当出口NO开始出现时,也检测到NO2的形成。最大值为~0.5ppm 在40 h时, 然后稳定在0.2 ppm。Co1Ni1在完全去除NOx的情况下显示出略微提高的效率,持续约30 h。该催化剂产生更高浓度的NO2,在~50 h时达到最大值。出乎意料的是,Co1Ni4的NO消除性能甚至低于纯Ni,显示出捕获效率的快速下降和在运行期间几乎瞬时释放NO2。 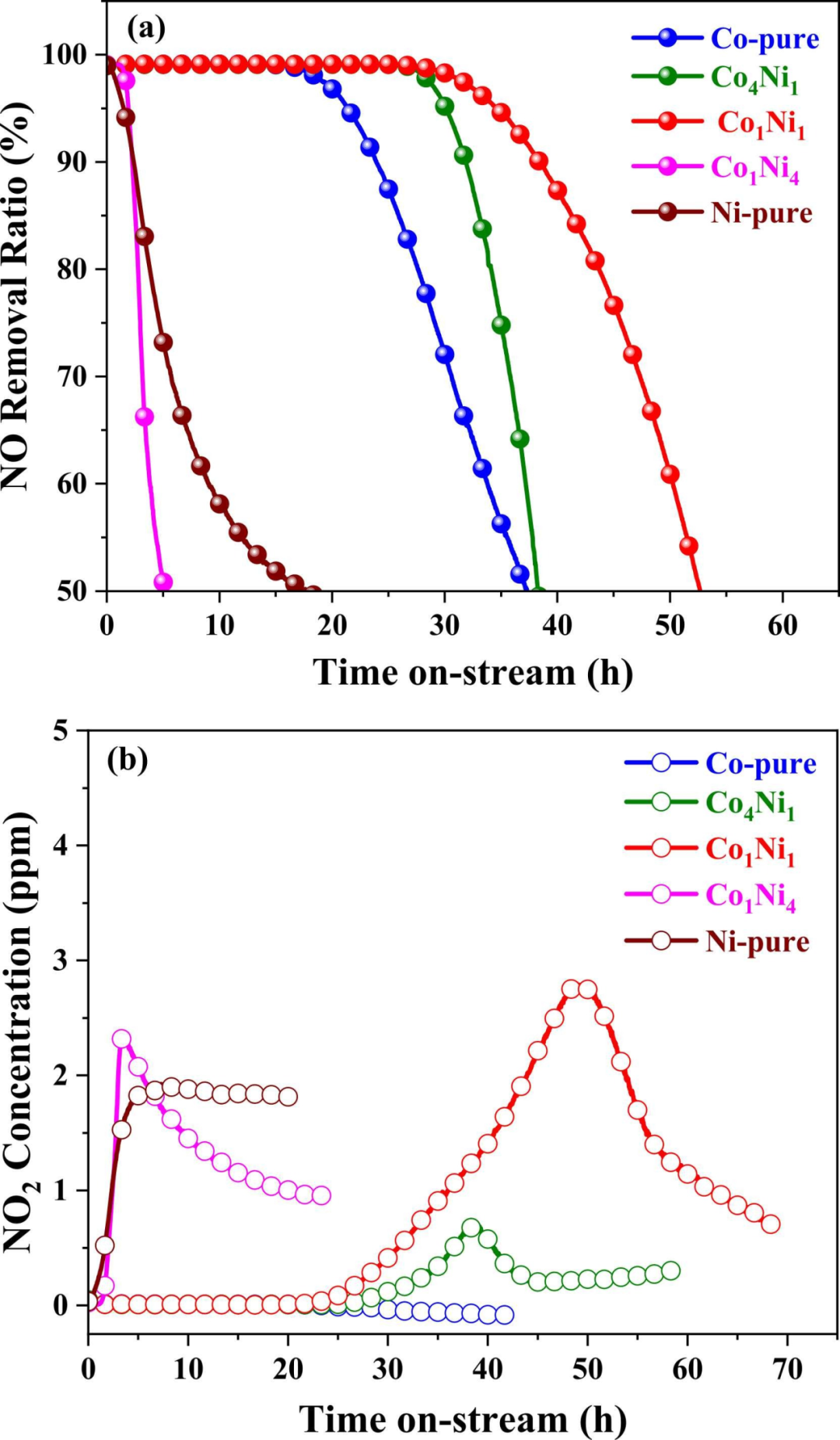 图1 CoxNiyOz·nH2O材料的NO去除率(a)和出口NO2浓度(b)。反应物原料气含有10 ppm的NO,21%的O2在120000 mL·g−1·h−1的WHSV下与Ar平衡,反应温度为25 °C 测试结果分析 进行原位DRIFTS以研究NO吸附产物的演变。图2(a-e)显示了在前30 min期间,分别在纯Co、Co4Ni1、Co1Ni1、Co1Ni4和纯Ni上记录的特征IR带的演变 NO吸附的分钟数(以5分钟间隔记录的光谱)。对于所有样品,可以很容易地观察到,在引入NO时形成新的IR带,并随着暴露时间的增加而增强。对于纯钴,在1337 cm−1和1415 cm−1对应于硝基配合物(-NO2)的对称和非对称拉伸。1190和1630 cm−1的较弱波段可分别归属于螯合硝基化合物和H2O的弯曲振动。由于离子硝酸盐通常在1420和1320 cm−1附近显示分裂的振动带和1030cm−1左右的对称弯曲模式,硝基配合物的IR带不容易与离子硝酸盐的IR带区分开来。因此,1420、1329和1030cm−1处的谱带被认为是由Co4Ni1的硝基化合物和离子硝酸盐共同贡献的。螯合硝基化合物(Γ = 1190 cm−1)和水( = 1630 cm−1)振动。由于亚硝酸盐和硝酸盐物种的共同沉积,Co1Ni1的红外光谱与Co4Ni1的红外谱相似。然而,观察到了一些细微的差异。1320-1420cm−1处的对称和非对称波段之间的分离的范围比Co1Ni1小,这可能是由于硝酸盐与亚硝酸盐的比例改变。此外,1630cm−1的谱带 和1190cm−1的螯合硝基带 与Co4Ni1相比,Co1Ni1上的减弱。此外,Co1Ni1上1286 cm−1处的肩带被认为是单齿硝酸盐,1566cm−1处的另一条带分别归属于双齿硝酸盐。总体而言,在Co1Ni1上观察到的IR带与XPS分析一致,这表明硝酸盐在Co1Ni 1上比在Co4Ni1和纯Co上更占主导地位。Co1Ni4的红外光谱在1384 cm−1处呈现一个突出的谱带和1286 cm−1的弱肩带,分别对应离子型硝酸盐和单齿型硝酸盐。1525、1286和971cm−1处的Ni纯带属于单齿硝酸盐。最后,注意到,在1950-2100 cm−1范围内,在纯Co(2060cm−1)宽带 ),Co4Ni1(2060 cm−1)和Co1Ni1(1955 cm−1)上形成,但在Co1Ni4和纯Ni上没有。这些带的性质并不完全清楚,但可能归因于这些材料微孔中NO和NO2物质的振动。为了直接比较5个样品,图2f总结了在30min NO/O2暴露的最小值。根据相对峰值强度,NO储存容量的顺序为Co1Ni1≈ Co4Ni1>纯 Co> 纯Ni≈ Co1Ni4。 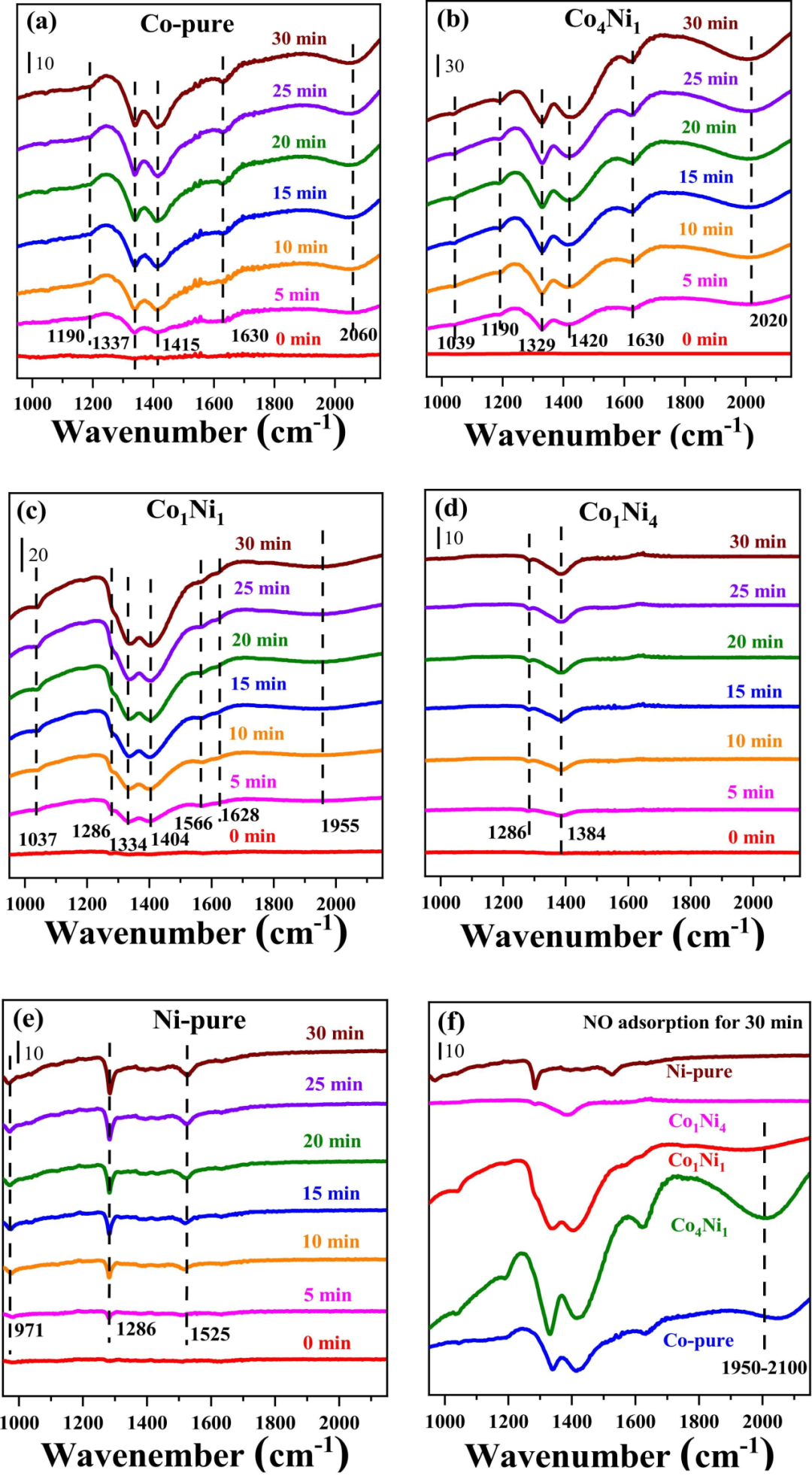 图2 NO/O2在纯Co(a)、Co4Ni1(b)、Co1Ni1(c)、Co1Ni4(d)和纯Ni(e)上吸附的原位DRIFT光谱;30分钟时的红外光谱 CoxNiyOz·nH2O材料上NO/O2暴露的最小值(f) 原位实验细节 原位DRIFTS和程序升温脱附(TPD)用于探测储存的含氮物种的性质。在带有MCT检测器的Nicolet Nexus 6700 FT-IR光谱仪上进行原位DRIFTS测量。在每次测试之前,样品在60℃下预处理1小时(50 mL·min−1的Ar作为平衡气体)。接下来,将样品冷却至25℃,然后与总流量为50 mL·min−1的原料气(500 ppm NO,21 vol% O2,Ar作为平衡气)反应。在4 cm−1的光谱分辨率下,用60次扫描的总和收集光谱,并且通过减去NO流动之前收集的背景光谱来获得所有光谱。在NO捕获试验50小时后,对使用过的样品进行TPD测量。在温度上升之前,用流动的Ar(300 mL·min−1)在25℃下吹扫样品1小时。随后,在相同的Ar流中以5℃/min的升温速率将样品从30℃加热到600℃,并在600℃下保持10分钟以完全去除NOx。通过NOx分析仪(Thermo Fisher 42i LS)实时记录出口NO和NO2的浓度。 4 结 论 合成了Co-Ni双金属水合氧化物(CoxNiyOz·nH2O)作为脱除空气中低浓度NO的捕集材料/催化剂。在这些材料中,这两种金属主要保持紧密混合的CoOOH和NiOOH部分。受Co/Ni原子比的强烈影响,近球形和片状晶粒之间的平衡是这些材料高表面积和低结晶度的关键。尽管这些材料的孔隙中可以捕获少量的NO和NO2,但NOx的储存主要是通过亚硝酸盐和硝酸盐的形成。基于原位DRIFTS、XPS和程序升温脱附研究,发现亚硝酸盐的形成与Co有关,硝酸盐的形成与Ni有关。还发现了一种协同作用,即Co上形成的亚硝酸盐被Ni上的晶格氧进一步氧化为硝酸盐。基于这些发现,提出了可能的亚硝酸盐和硝酸盐形成化学物质。本文研究的一些双金属含水氧化物,例如Co1Ni1,在环境温度下显示出显著的NO捕获效率,因此具有很大的应用潜力。最后,即使热再生不能应用于这些结晶性差的材料,用Na2S2O8水溶液洗涤也很容易恢复它们的捕获能力。 原文链接: Bo Lin, Ziwei Bao, Aiyong Wang, et al.An efficient Co-Ni hydrous oxide catalyst for elimination of NO pollutant in semi-enclosed spaces at ambient temperature. Applied Catalysis B: Environmental 337 (2023) 122984 DOI:10.1016/j.apcatb.2023.122984 https://doi.org/10.1016/j.apcatb.2023.122984 |
||
|
版权所有 © 2014 华东理工大学工业催化研究所 |